為了把關生物藥品的安全與品質,藥事法第74條訂出嚴謹的規範,規定每批生物藥品在輸入或製造後若無經「中央衛生主管機關」抽樣、檢驗合格並加貼查訖封緘,不得進行銷售。
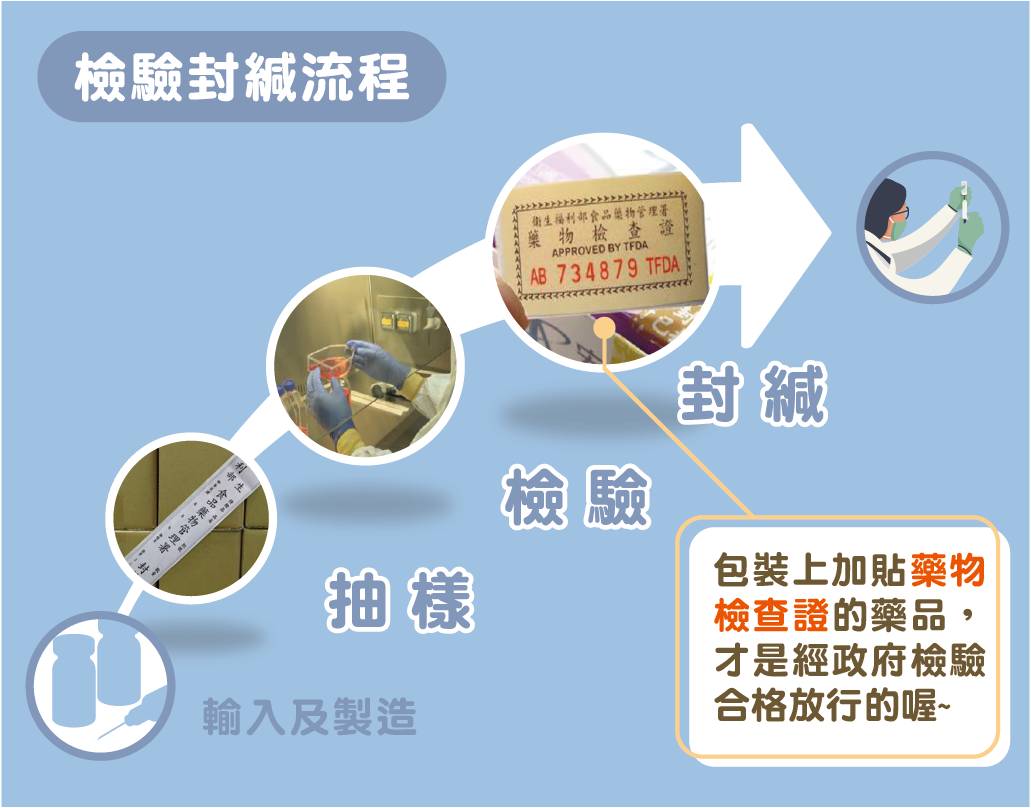
食藥署進一步說明,整個檢驗封緘流程可分成三步驟:抽樣、檢驗審查與封緘:
一、抽樣
生物藥品輸入或製造後需要填寫「生物藥品檢驗封緘申請書」,並檢附包裝清單、藥品許可證,或經中央衛生主管機關核可文件、檢定合格證明、製程、檢驗方法、規格、標準品、原料來源證明、分裝及檢定紀錄等資料給食藥署,當食藥署收到檢驗封緘申請後,會派員針對藥品運送及儲存條件做查核,確認符合規範後,抽取樣品並原地封存剩餘藥品後,攜回樣品做檢驗。
二、檢驗與審查
帶回的檢品由食藥署國家級實驗室針對安全性、效價、鑑別、化學試驗分別進行檢驗,並審查廠商檢附之申請文件,確認其品質與安全性符合規定。
三、封緘
檢驗合格的產品會核發生物藥品封緘證明書,並在每個藥品的最小包裝上貼上「藥物檢查證」後才會放行。黏貼藥物檢查證後的生物藥品代表經過國家的嚴格把關,除了可供醫療院所做為識別依據,也有利後續追蹤,當特定批號出現疑慮時,才能精準掌握流向。
由於生物製藥很容易受到環境變化而產生影響,透過三個嚴謹的審核機制,可確保不同批次的產品品質擁有一致性,且運送過程沒有造成不良影響。食藥署再次強調,只要是藥品,不論是新藥、學名藥、生物藥品或甚至製造藥品的原料,都會經過國家衛生主管機關查驗登記審查或因應緊急事態依藥事法第48-2條取得專案核准後,始得製造或輸入。
✲ 摘自衛生福利部食品藥物管理署 藥物食品安全週報 第856期https://www.fda.gov.tw/tc/PublishOtherEpaperContent.aspx?id=1391&tid=3788&r=2068584843✲